Попередня сторінка: Насичені одноатомні спирти: фізичні т�...
Наступна сторінка: Багатоатомні спирти. Гліцерол
Пригадайте: формули для обчислення масової частки розчиненої речовини та формули для обчислення кількості речовини.
Обчислення даних про продукт реакції, якщо реагент містить домішки
Цей алгоритм застосовують, якщо за умовою задачі:
• відома масова частка домішок у реагенті;
• домішки не вступають у хімічну реакцію;
• необхідно обчислити масу, або об’єм, або кількість речовини продукту реакції чи одного з чистих реагентів.
Більшість реагентів, що використовують для проведення хімічних реакцій, як і більшість речовин у природі, є не чистими речовинами, а сумішами кількох речовин. За вмістом домішок речовинам надають певну кваліфікацію чистоти: чиста («Ч»), хімічно чиста («ХЧ»), чиста для аналізу («ЧДА») тощо. В усіх чистих реагентах уміст домішок не більше 1 %, тому для розрахунків ними можна нехтувати. Але чисті речовини досить дорогі, тому їх використовують переважно для дослідів у лабораторії, де витрачають у невеликих кількостях.
У промисловості, де ціна реагентів істотно впливає на рентабельність виробництва, зазвичай використовують не дуже чисті реагенти. Про такі речовини говорять, що вони «технічно чисті», наприклад технічний кальцій карбід або технічний бензен. Уміст домішок у них може бути кілька відсотків, а іноді й значно більше.
За алгоритмом розв’язання такі задачі подібні до задач, у яких реагенти розчинені у воді й відома їхня масова частка в розчині. А розрахункові формули для обчислення масової частки домішок та масової частки розчиненої речовини подібні. Порівняйте!
Для обчислення масової частки розчиненої речовини:

І, певна річ, сума масових часток чистої речовини та домішок у технічному реагенті має дорівнювати 1 (або 100 %):

Задача 1. Обчисліть масу хлоробензену, що можна добути з технічного бензену масою 150 г, у якому масова частка домішок 6,4 %.
Розв’язання:
Спочатку визначаємо масу чистого бензену. За формулою (4) обчислюємо масову частку чистого бензену:
^(бензену) = 1 - ^(домішок) = 1 - 0,064 = 0,936.
Перетворюємо формулу (2) та обчислюємо масу чистого бензену: т(чистого реагенту) = ^(чистого реагенту) ■ т(техн. реагенту) m(C6H6) = т(техн. C6H6) ■ w(C6H6) = 150 г ■ 0,936 = 140,4 г.
Далі задачу розв’язуємо як звичайну задачу на обчислення за рівняннями хімічних реакцій. Визначаємо кількість речовини бензену:

У рівнянні реакції коефіцієнти перед бензеном та хлоробензеном однакові (дорівнюють 1):

Отже, кількості речовини бензену та хлоробензену також однакові:

Останнім етапом обчислюємо масу продукту реакції:

Обчислення масової частки домішок у реагенті
Цей алгоритм застосовують, якщо за умовою задачі:
• необхідно обчислити масову частку домішок або чистої речовини в реагенті;
• відомо, що домішки не вступають у хімічну реакцію, тобто є інертними;
• відома маса, або об’єм, або кількість речовини продукту реакції;
• відома маса реагенту технічного ступеня чистоти.
Задача 2. Обчисліть масову частку домішок у технічному про-панолі, якщо під час згоряння його зразка масою 2 г виділився вуглекислий газ об’ємом 1,68 л (н. у.).
Розв’язання:
Такі задачі можна розв’язати, якщо домішки є інертними, тобто в даному випадку домішки не мають горіти. І хоча в умові задачі про це прямо не йдеться, але мається на увазі. В іншому випадку задачу розв’язати неможливо. Якщо домішки є інертними, то вуглекислий газ виділяється лише внаслідок згоряння пропанолу, тому, знаючи об’єм вуглекислого газу, обчислимо масу чистого пропанолу. Кількість речовини вуглекислого газу:
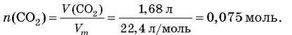
За рівнянням реакції горіння пропанолу

визначаємо, що співвідношення кількості речовини пропанолу та вуглекислого газу:

Маса чистого пропанолу

Обчислення маси реагенту, що містить домішки, необхідного для проведення реакції
Цей алгоритм застосовують, якщо за умовою задачі:
• необхідно обчислити масу реагенту технічного ступеня чистоти;
• домішки не вступають у хімічну реакцію, тобто є інертними;
• відома маса, або об’єм, або кількість речовини продукту реакції;
• відома масова частка чистого реагенту в суміші.
Цей тип задач частіше трапляється в роботі технологів на великих підприємствах, коли є потреба визначити, в якій кількості необхідно завантажити реагенти в реактор, якщо відомо, скільки готової продукції необхідно отримати.
Задача 3. Деякі спиртові заводи в Україні для виробництва етанолу використовують цукровий очерет. Середній уміст цукру в очереті становить 15 %. Обчисліть масу такого очерету, що знадобиться для добування етанолу об’ємом 1150 л (густина 0,8 г/см3). Припустіть, що очерет містить тільки глюкозу.
Розв’язання:
Примітка: хоча в одиницях CI об’єм та густина вимірюються в м3 та кг/м3 відповідно, але традиційно в хімічних розрахунках використовують кратні одиниці мл та г/мл. Головне під час розрахунків, щоб одиниці вимірювання всіх величин були однаковими.
F(C2H5OH) = 1150 л або 1,15 ■ 106 мл; p(C2H5OH) = 0,8 г/см3, або 0,8 г/мл. У цій задачі очерет — це технічний реагент, а глюкоза, що в ньому міститься,— чиста речовина. Щоб визначити масу очерету, якого вистачить для добування 1150 л спирту, насамперед необхідно знати, скільки глюкози він має містити. Обчислимо це, знаючи, що етанол утворюється тільки внаслідок бродіння глюкози. Обчислюємо кількість речовини етанолу:


Ключова ідея
Математично масова частка домішок ідентична масовій частці розчиненої
речовини в розчині.
Завдання для засвоєння матеріалу
225. Обчисліть об'єм етену, який можна добути з технічного етанолу масою 250 г, що містить 8 % домішок.
226. Природний газ об'ємом 1 м3 (н. у.), що містить 10,4 % домішок азоту (за об'ємом), піддали піролізу. Обчисліть максимальний об'єм етину, що можна добути.
227. Під час згоряння технічного бензену масою 1 г утворився вуглекислий газ масою 2,64 г. Обчисліть масову частку домішок у бензені.
228. З вуглецю масою 1 кг добуто метан об'ємом 1,792 м3 (н. у.). Обчисліть масову частку домішок у вуглецю.
229. Із глюкози масою 1,1 кг добуто етанол об'ємом 0,69 л (густина 0,8 г/см3). Обчисліть масову частку домішок у глюкозі.
230. Технічний кальцій карбід масою 1,6 г залили надлишком води. Під час пропускання утвореного газу крізь розчин брому в реакцію вступив бром масою 7,2 г. Обчисліть масову частку домішок у технічному кальцій карбіді.
231. Обчисліть масу технічного бензену з масовою часткою домішок 6,4 % для добування бромобензену масою 565,2 г.
232. Технічний етанол містить 4 % домішок. Обчисліть масу зразка такого етанолу, якщо під час його згоряння утворився вуглекислий газ масою 0,9183 г.
Міні-проекти
233. Дізнайтеся з відкритих джерел інформації про хімічні або харчові виробництва, що є у вашій місцевості: яку продукцію вони випускають, яку сировину використовують та приблизні обсяги виробництва. Уявіть, що ви працюєте головним технологом на цьому підприємстві та контролюєте аналітичну лабораторію. Змоделюйте ситуацію, за якої в лабораторії припустилися помилки у визначенні вмісту корисної речовини в сировині (у більший або в менший бік). Оцініть, як це відіб'ється на прибутках вашого підприємства.
Це матеріал з підручника Хімія 10 клас Григорович
Наступна сторінка: Багатоатомні спирти. Гліцерол